Inhoud
In de chemie verwijst het concept van polariteit naar hoe sommige chemische bindingen leiden tot een ongelijke verdeling van elektronen. Dit betekent dat gedeelde elektronen dichter bij het ene atoom in een binding staan dan het andere, waardoor gebieden met positieve en negatieve lading ontstaan. Je kunt het verschil in elektronegativiteit van twee atomen gebruiken om te voorspellen of ze polaire, niet-polaire of ionische bindingen maken. Water is een bekend voorbeeld van een polair molecuul. Volgens de Universiteit van Arizona heeft "Water een gedeeltelijke negatieve lading nabij het zuurstofatoom - en gedeeltelijk positieve ladingen nabij de waterstofatomen."
Teken de Lewis-structuur van het molecuul. Let op elk element in het molecuul.
Zoek elk element in het molecuul op in een elektronegativiteitstabel en noteer hun elektronegativiteit.
Trek de elektronegativiteit van het ene atoom in een binding af van het andere. Neem de absolute waarde. Een verschil van 0,0 tot 1,2 is niet-polair. Een verschil van 1,2 tot 1,8 is polair. Een verschil van 1,8 en meer is ionisch.
Herhaal stap 3 voor elke binding in het molecuul.
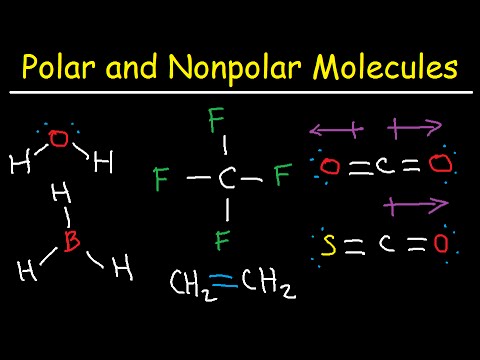
Teken een pijl in de buurt van elke poolverbinding. Richt de punt op het meer elektronegatieve atoom. Als alle pijlen naar een gemeenschappelijk centrum wijzen, is het molecuul niet-polair. Als ze dat niet doen, is het molecuul polair.